
Błony modelowe. Liposomy
Błony modelowe są to sztuczne układy przypominające swoją budową naturalne błony biologiczne, dzięki czemu są pomocne w badaniach ich struktury i dynamiki molekularnej. Układy modelowe obejmują wodne układy cząsteczek surfaktantów (np. micele, monowarstwy), mono- i wielowarstwy zbudowane z lipidów oraz błony płaskie i liposomy (sferyczne dwuwarswy lipidowe). Jednym z ważniejszych praktycznych zastosowań błon lipidowych układów modelowych, w szczególności liposomów jest transport substancji aktywnych w danej strukturze lub w organizmie.
Budowa liposomów
Liposomy są to pęcherzykowate zamknięte struktury utworzone z dwuwarstwy lipidowej, budową najbardziej zbliżone do błon biologicznych. Ich wnętrze wypełnia faza wodna. Posiadają charakter koloidów i stabilizowane są przez siły napięcia powierzchniowego, a tworzone są w wyniku hydratacji fosfolipidów, wykazujących właściwości amfifilowe. Właściwości te wynikają z obecności warstwy hydrofilowej („polarna głowa”) i hydrofobowej („niepolarny łańcuch alkilowy”) [32]. W środowisku wodnym dwuwarstwa lipidowa powstaje szybko, co wiąże się z oddziaływaniami hydrofobowymi. Dodatkowo otrzymane struktury stabilizowane są przez siły van der Waalsa (między łańcuchami węglowodorowymi), oddziaływania elektrostatyczne oraz wiązania wodorowe [30].
Skład liposomów może być zmieniany, poprzez wbudowywanie dodatkowych lipidów (np. cholesterolu, glikolipidów), które nadają im większą stabilność in vivo i in vitro oraz lipidów naturalnie występujących w błonach naturalnych, m.in. PC i fosfatydyloetanoloaminy (PE). Dodatek białek jest pomocny w kierowaniu liposomów do danej tkanki docelowej [32]. Obecnie udaje się otrzymywać liposomy składem bardzo przypominające naturalne błony biologiczne [33].
Klasyfikacja i otrzymywanie poszczególnych klas liposomów
Istnieje wiele metod otrzymywania liposomów, zależnie od tego jakie struktury spełniają wymagania odpowiadające danemu zastosowaniu. Trzy główne klasy liposomów (Rys. 5.2) stosowane powszechnie to:
liposomy wielowarstwowe MLV (ang. multi lamellar vescicles);
liposomy duże jednowarstwowe LUV (ang. large unilamellar vescicles);
liposomy małe jednowarstwowe SUV (ang. small unilamellar vescicles) [33].
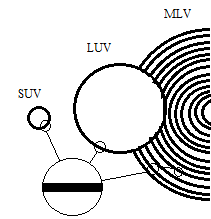
Rys. 5.2. Trzy główne klasy liposomów [33]
MLV wykorzystywane są do zamykania substancji rozpuszczonej (solwentu), gdy nie ma narzuconych ograniczeń związanych z budową i rozmiarem liposomów oraz kiedy nie stawiane są wymogi dotyczące efektywności zamykania roztworów wodnych. Zależnie od tego na jaką skalę tworzone mają być omawiane struktury, różne są metody ich otrzymywania. W laboratorium wykorzystuje się metodę hydratacji cienkiego filmu lipidowego, zaś do produkcji na większą skalę korzysta się z metod typu: liofilizacja, suszenie z odparowaniem rozpuszczalnika [33].
LUV to liposomy ważne zwłaszcza przy zamykaniu solutów obecnych w warstwie wodnej (metoda: odparowanie fazami odwróconymi). Stosuje się je również w rekonstrukcji białek błonowych (metody usuwania detergentów) oraz do badań związanych z przepuszczalnością i fuzją błon [33].
SUV dzięki małym rozmiarom są często stosowane, gdy nie jest wymagana znaczna wydajność zamykania hydrofilowych solutów. Na skalę laboratoryjną przygotowuje się je wykorzystując ultradźwięki, prasę Frencha albo wstrzykiwanie roztworów etanolowych [33].
Właściwości i zastosowanie liposomów
Liposomy są szeroko stosowane dzięki możliwości ich uzyskania jako bardzo zbliżonych pod względem budowy do błon biologicznych. Pozwalają badać właściwości białek błonowych oraz procesów zachodzących w komórkach [33]. W związku z tym, że stanowią jeden z najlepszych układów modelowych, umożliwiają badanie przepuszczalności błon. Właściwości takie jak: nietoksyczność, biodegradowalność oraz zdolność tworzenia fuzji z błonami komórkowymi, przyczyniają się do wykorzystywania liposomów do transportu danych substancji aktywnych w strukturach tkankowych organizmów. Przekazywanymi składnikami mogą być np. leki zamknięte w warstwie wodnej lub wbudowane w warstwę dwulipidową [32].
Liposomy znalazły także zastosowanie w badaniach dotyczących cyklu ksantofilowego okrzemek. Wykorzystywano je m.in. w badaniach przebiegu reakcji deepoksydacji przeprowadzanych in vitro [28].
komentarze
Copyright © 2008-2010 EPrace oraz autorzy prac.