
Budowa okrzemkowych fotoukładów i ich anten energetycznych
Budowa aparatu fotosyntetycznego okrzemek różni się od tego występującego u roślin wyższych brakiem rozgraniczenia na tylakoidy gran i stromy. Główne kompleksy zbierające światło to kompleksy FCP wiążące Chla i Chlc oraz Fx. W przeciwieństwie do roślin wyższych, gdzie LHC II znajduje się w granach tylakoidów, FCP u okrzemek rozmieszczone są w tych strukturach równomiernie [16].
Kompleksy FCP należą do rodziny kompleksów zbierających światło i wykazują wiele podobieństw do LHC II roślin wyższych [16]. Jednak główną różnicą jest skład barwnikowy. Antenę chlorofilową stanowi Chlc. Najważniejszym karotenoidem zbierającym światło jest Fx. W mniejszym stopniu obecne są barwniki cyklu diadinoksantynowego, które absorbują światło w zakresie 450 – 580 nm (nawet w głębokich warstwach zbiorników wodnych) [25]. Ostatnio udało się określić model barwnikowej stechiometrii FCP PS II okrzemek. Uważa się, że na każdy monomer FCP przypada osiem cząsteczek Chla, osiem cząsteczek Fx i dwie cząsteczki Chlc. Monomery te tworzą później trimery i oligomery w antenie peryferyjnej PS II. Niedawno przeprowadzone badania pozwoliły stwierdzić, że skład barwnikowy podjednostek kompleksu antenowego PS I jest zgodny z tym zawartym w monomerze FCP PS II [5].
Główne barwniki cyklu ksantofilowego odpowiedzialne za ochronę przed szkodliwym promieniowaniem słonecznym to Ddx oraz Dtx. Monomer FCP posiada co najmniej jedną związaną cząsteczkę Ddx [5, 26]. Ddx rozpuszczona jest w warstwie lipidowej otaczającej kompleksy FCP, dzięki czemu w obecności intensywnego światła, w łatwy sposób może ulegać deepoksydacji. Uważa się, że barwniki cyklu diadinoksantynowego występujące w otoczeniu lipidowym FCP pełnią funkcję fotoprotektorów w tym antyoksydantów, a według jednej z hipotez mogą stanowić rezerwuar do syntezy Fx [5].
Na rysunku 4.7. przedstawiono schemat fotoukładów występujących u okrzemek typu T. pseudonana. Udało się poznać skład białkowy membran ich tylakoidów. PS II występuje u nich w formie dimeru, natomiast PS I jako monomer. Podjednostki wchodzące w skład PS I to krótkie polipeptydy: PsaA, PsaL, PsaB, PsaF, PsaE, PsaJ, PsaM i PsaI. PS II zawiera kompleks wiążący tlen (PsbO, PsbU, PsbV, PsbQ i Psb31) [27].
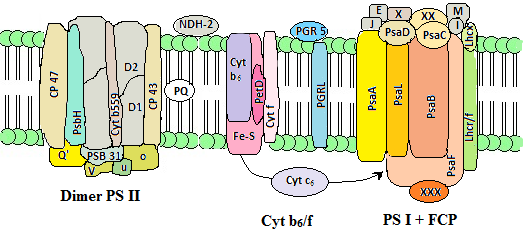
Rys. 4.7. Schemat budowy kompleksów białkowych membran tylakoidów u okrzemek rodzaju T. pseudonana. [27]
Okrzemki Phaeodactylum tricornutum posiadają tylko jeden rodzaj anteny FCP, która tworzy trimer. Jednak możliwa jest jego izolacja w postaci oligomeru przy zastosowaniu delikatnych warunków rozpuszczalnikowych [26].
W genomie okrzemek zakodowane są trzy podstawowe rodziny białek antenowych:
„klasyczne” białka zbierające światło – Lhcf;
białka Lhcr związane z LHC I krasnorostów;
białka Li818 zwane Lhcx.
Dowiedziono, że Lhcf i Lhcr występują w chloroplastach okrzemek w podobnych ilościach, a zawartość Lhcx jest znacznie niższa. W kompleksie FCP P. tricornutum znaleziono 12 z 15 białek Lhcf oraz 7 z 14 białek Lhcr [26].
Dodatkowo, okrzemki zawierają specyficzny kompleks FCP związany z PS I. Zawiera on więcej związanych cząsteczek Ddx i znacznie mniej Fx niż główny FCP. FCP I jest w bardzo dużym stopniu zbudowany z białek Lhcr, które są ściśle związane z anteną PS I krasnorostów i kryptofitów. Funkcje FCP I nadal nie są dokładnie poznane [26].
komentarze
Copyright © 2008-2010 EPrace oraz autorzy prac.